Smeltend ijs
Smeltend ijs
Help, de zeespiegel stijgt!
Marjan Waldorp
Angst
Klimaatactivisten jagen ons graag angst aan met verhalen over smeltende poolkappen en daaruit voortvloeiende zeespiegelstijgingen. In het jaar 2100 zou als gevolg van klimaatverandering de zeespiegel wel met zeven meter, volgens sommigen zelfs met honderd meter kunnen stijgen. Heel effectieve angstpropaganda! Verdrinkingsangst is ons allen immers aangeboren.
Maar kunnen de poolkappen wel zo makkelijk smelten? Of maken de klimaatactivisten dankbaar gebruik van het feit dat de gemiddelde burger de meest elementaire natuurkundige kennis ontbeert?
Niet temperatuur maar energie!
Uit ervaring weten we allemaal dat wanneer de lucht buiten opwarmt sneeuw en ijs gaan smelten. (En dat is waar de klimaatactivisten handig op inspelen!) Wat de oppervlakkige waarnemer zich echter niet realiseert is dat dit smeltproces een voortdurende toevoer van energie vereist! Zonder een voortdurende toevoer van verse warme lucht zal de omgevingslucht snel afkoelen tot 0°C en het smeltproces stoppen. Voor smelten is energie het sleutelwoord, niet temperatuur!
Laten we eens het volgende gedachte experiment doen. Stel we nemen een bakje ijs van 0°C en plaatsen dit op een warmtebron. We verwarmen het ijs net zolang tot alle ijs gesmolten is tot water van 0°C en noteren de verstreken tijd. Vervolgens laten we het verwarmingsproces met exact dezelfde tijd nog eens verder lopen. Tot hoeveel °C is het smeltwater nu opgewarmd?
- a) 5,9°C
- b) 20,3°C
- c) 79,7°C
Om het juiste antwoord te vinden moeten we weten hoeveel warmte er nodig is om ijs te smelten en hoeveel warmte er nodig is om water in temperatuur te doen stijgen. In Wikipedia vinden we dat de smeltwarmte van ijs 334 Joule per gram bedraagt. 1 De hoeveelheid warmte die nodig is om 1 g water 1°C te verwarmen, weten we uit de middelbare school natuurkunde lessen: 1 Calorie. De Calorie is echter uit de mode geraakt en vervangen door de officiële SI-eenheid voor energie de Joule (J). 2 Eén Calorie is ongeveer 4,19 Joule. Dus:
- Benodigde energie om ijs van 0°C te smelten: 334 J/g
- Benodigde energie om water op te warmen: 4,19 J/g°C
Met deze gegevens kunnen we berekenen dat wanneer we aan smeltwater van 0°C dezelfde hoeveelheid energie toevoeren als benodigd om ijs van 0°C te smelten het smeltwater zal worden opgewarmd met:
(334 J/g) / (4,19 J/g°C) = 79,7°C
Ja, ongelofelijk, maar waar: Het smelten van ijs komt overeen met een temperatuursprong van bijna 80°C! Het omzetten van water in de vaste vorm (ijs) naar de vloeibare vorm, de z.g. faseverandering, vraagt enorm veel energie. Bij het omgekeerde proces, van vloeibaar naar vast (bevriezen), komt enorm veel energie (warmte) vrij.
Onderstaande grafiek laat de energie zien, die nodig is om diepgevroren ijs van -25°C op te warmen tot het smeltpunt van 0°C, het ijs te smelten en vervolgens het smeltwater op te warmen tot 100°C:
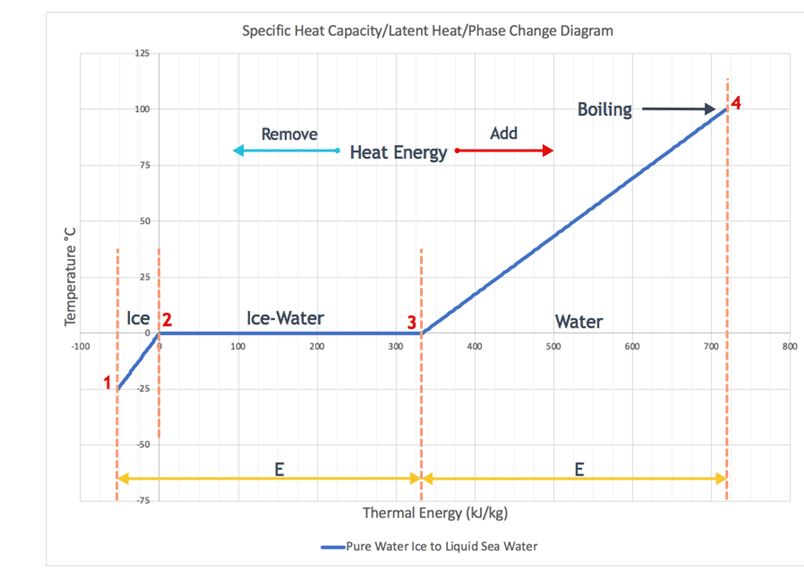
Bron: wattsupwiththat.com 3
Stabiel aards klimaat
Voor zijn boekje "Blauwe Planeet (Niet Groen)" 4 vroeg Václav Klaus het Tsjechisch Instituut voor de Hydrometeorologie een willekeurige tijdreeks van een door hen uit te kiezen meetstation, dat reeds gedurende een lange periode actief is. Ze stuurden hem de meetgegevens van de stad Opava. In het boekje staat een puntenwolk afgebeeld met de jaargemiddelden over de periode 1921-2006. 5 Wat opvalt is de enorme variatie. In 1932 was de gemiddelde temperatuur 10,2°C, in 1940 5,9°C, in 1995 6,8°C en in 2000 9,9°C. Op het oog valt er geen trend waar te nemen. Via regressie-analyse blijkt de trend +0,28°C per eeuw te zijn. De inwoners van Opava zullen die trend echter niet zo aan den lijve ervaren.
Kleine geleidelijke temperatuurveranderingen op lange termijn en grote temperatuurfluctuaties op korte termijn is een goede karakterisering van het aardse klimaat. Beide kenmerken zijn ook fysiek aan te wijzen: enerzijds water in al zijn vormen op aarde en anderzijds de atmosfeer. In vergelijking met andere ons bekende planeten is planeet aarde uniek in haar grote hoeveelheid water en ijs. Het aardoppervlak is voor 71% met water bedekt. De gigantische hoeveelheid water in alle oceanen, de enorme ijsmassa's aan de polen en de voortdurende faseveranderingen tussen ijs, water en waterdamp, geven de aarde een enorme energie-opslag, een warmte-accu. Die warmte-accu maakt grote temperatuurveranderingen op korte tijd onmogelijk!
Daarnaast is de aarde omgeven door een ijle luchtlaag, de dampkring of atmosfeer. In vergelijking tot de oceanen heeft de atmosfeer een hele geringe warmtecapaciteit! De soortelijke warmte van oceaanwater is 3,85 J/g°C. De soortelijke warmte van lucht is ongeveer 1 J/g°C. 6 De soortelijke warmte van lucht is dus bijna 4x lager dan die van oceaanwater. Echter wanneer we het over lucht hebben denken we niet in massa (kg), maar in volume (m3). En dan telt dat lucht zo'n lage soortelijke massa heeft!
Op zeeniveau (1 bar) is de soortelijke massa van lucht 1,29 kg/m3. Op 5500 m hoogte is de luchtdruk echter al tot de helft gedaald (0,5 bar) en is de soortelijke massa nog maar 0,65 kg/m3. Tussen de 0 en 5500 m hoogte is lucht dus 775-1550x lichter dan water! In volume gezien is de soortelijke warmte van lucht daardoor 3000-6000x kleiner dan water! Dat verklaart waarom lucht zo snel kan opwarmen en afkoelen. Op een zonnige dag warmt de buitenlucht gemakkelijk met 4°C per uur op:
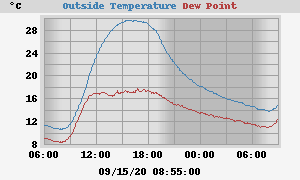
Bron: weerstation auteur
Atmosfeer speelbal van natuurkrachten
Ondanks de massale aandacht die klimaatactivisten aan de dag leggen voor de atmosfeer en ondanks de miljarden dollars en euro's die jaarlijks besteed worden aan de bestudering van haar marginale temperatuurtrends, speelt de atmosfeer in de energiebalans van de aarde nauwelijks een rol! Anthony Watts rekent op zijn klimaatsite "Watts Up With That" uit dat de warmtecapaciteit van de oceanen ongeveer 1100x zo groot is als die van de atmosfeer. 7 Stel dat er zoveel energie uit de oceanen zou vrijkomen dat de gemiddelde temperatuur van de atmosfeer zou stijgen van 15°C (heden) naar 26°C - een extreme klimaatopwarming! De gemiddelde temperatuur van de oceanen zou dan dalen met 0,01°C. Vrijwel nihil dus, een uitdaging om vast te stellen!
Met zijn lage soortelijke warmte en geringe warmtecapaciteit is de atmosfeer een gemakkelijke speelbal in handen van de diverse natuurkrachten. Hij reageert gevoelig en snel op bijv. veranderingen van:
- zoninstraling
- reflectie van het aardoppervlak
- wolkenvorming
- verdamping, convectie en condensatie 8
- broeikasgassen (waterdamp, methaan, CO2, etc.)
- aerosolen (bijv. door vulkaan uitbarstingen)
- zeestromingen
- aardwarmte
Smeltende poolkappen
Van al het landijs op aarde bevindt zich ca. 91% op Antarctica, 8% op Groenland en 1% verspreid over de rest van de wereld. 9 Stel dat door klimaatopwarming de Groenlandse ijskap zou smelten. Met hoeveel °C zou de atmosfeer dan dalen, wanneer de benodigde smeltwarmte aan de atmosfeer onttrokken zou worden?
| Smeltwarmte Groenlandse ijskap | ||
|---|---|---|
| Volume: | ca. 2,6 x 106 km3 | = 2,6 x 1018 dm3 |
| Massa: | 2,6 x 1018 dm3 x 0,9167 kg/dm3 | = 2,38 x 1018 kg |
| Smeltwarmte: | 2,38 x 1018 kg x 334 kJ/kg | = 795 x 1018 kJ |
| Afkoeling atmosfeer | ||
| Massa: | 5,1 x 1018 kg | |
| Warmtecapaciteit: | 5,1 x 1018 kg x 1 kJ/kg°C | = 5,1 x 1018 kJ/°C |
| Afkoeling: | 795 x 1018 kJ / 5,1 x 1018 kJ/°C | = 156°C |
Ten gevolge van de onttrokken smeltwarmte zou de atmosfeer dus met 156°C
dalen.
In deze berekening is nog niet meegenomen de energie, die nodig is om het
diepgevroren ijs van ca. -25°C op de warmen tot het smeltpunt:
| Opwarming ijs -25°C tot 0°C | ||
|---|---|---|
| Energie: | 25°C x 2,108 kJ/kg°C | = 52,7 kJ/kg |
| Percentueel: | 52,7 kJ/kg / 334 kJ/kg | = +16% |
Inclusief de opwarming van het ijs tot het smeltpunt zou de gehele aardse
atmosfeer met 180°C dalen. Om de ijskap te kunnen smelten, hebben we
echter een stijging van de temperatuur in de atmosfeer nodig, geen daling.
Het effect van de door de mens veroorzaakte broeikasgassen zou deze daling
dus met meer dan 180°C moeten compenseren!
Wanneer we deze berekening herhalen voor het smelten van alle poolijs in de wereld, dus niet alleen Groenland maar ook Antarctica, waar veruit het meeste ijs ligt opgeslagen, dan leidt dit tot draconische cijfers. Het effect van broeikasgasen zou dan een afkoeling van 2560°C moeten compenseren! Ik laat het aan de lezer te beoordelen of dergelijke scenarios op een -geologisch gezien- korte termijn realistisch zijn, of dat we hiermee het domein van het bovennatuurlijke zijn binnengetreden.
-
SI: Système international d'unités 1960
wikipedia: Joule - 1 J = 1 wattseconde (Ws) ↩ -
wattsupwiththat: 4-keys-to-melt-fears-about-ice-sheets-melting
climategate: basisberekeningen-voor-het-smelten-van-de-poolkappen ↩ -
Blauwe Planeet (Niet Groen) blz. 87, Václav Klaus 2007-2010 ↩
-
De soortelijke warmte van oceaanwater is iets lager dan die van zuiver water: 3,85 J/g°C i.p.v. 4,19 J/g°C. wikipedia: Soortelijke Warmte ↩
-
De verdampingswarmte van water is 2256 J/g, 6,75x de smeltwarmte! Door verdamping worden enorme hoeveelheden energie aan het aardoppervlak onttrokken. In de hogere luchtlagen komt deze warmte via condensatie weer vrij. Volgens Prof. Richard Lindzen is het warmtetransport door convectie 100x zo groot als dat door straling. Als dat waar is, is de discussie over broeikasgassen een nondiscussie. GWPF: prof. Richard Lindzen, Global Warming For The Two Cultures, Oct. 2018 ↩